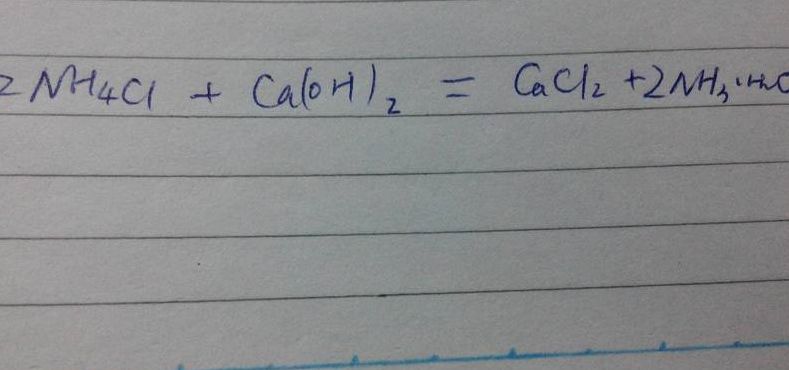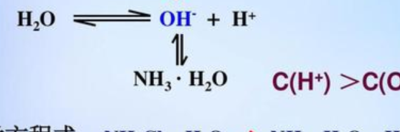氯化铵的水解方程式怎么写?
氯化铵水解方程式是:NH4Cl+H2ONH3·H2O+HCl。因为在水中电离出的铵根离子水解使溶液显酸性,常温下饱和氯化铵溶液pH值一般在6左右。25℃时,1%为5,3%为1,10%为0。
水解方程式如下图:水解是一种化工单元过程,是利用水将物质分解形成新的物质的过程。通常是指盐类的水解平衡。盐类的水解就是指盐中的弱碱阳离子或者酸根离子与水电离产生的氢离子或者氢氧根离子结合,生成弱电解质的过程。
氯化铵水解离子方程式是NH4++H2O可逆生成NH3*H20+H+。氯化铵简称氯铵,是指盐酸的铵盐,多为制碱工业的副产品。
NH4Cl水解离子方程式:氯化铵为无色晶体或白色结晶性粉末;无臭,味咸、凉;有引湿性。本品在水中易溶,在乙醇中微溶。水溶液呈弱酸性,加热时酸性增强。
氨水不水解(铵盐才水解)。氨水的电离方程式为:NH·HO=可逆=NH+十OH- 氨水有一定的腐蚀作用,碳化氨水的腐蚀性更加严重。对铜的腐蚀比较强,钢铁比较差,对水泥腐蚀不大。
防止氯化铵水解,pH调多少最好?
1、加热时酸性增强。因为NH4Cl在水中电离出的铵根离子水解使溶液显酸性,常温下饱和NH4Cl溶液PH值一般在6左右。25℃时,1%为5,3%为1,10%为0。
2、氨—氯化铵缓仲液 pH0:取氯化铵 07g,加水使溶解成100ml,再加稀氨溶液1→30调节pH值至0,即得。
3、。水溶液的pH:因为在水中电离出的铵根离子水解使溶液显酸性,常温下饱和氯化铵溶液PH值一般在6,1mol/L的氯化铵PH约为5,说明溶液是酸性,在相同条件下,氨水的导电性比强碱溶液弱,氨水受热分解挥发出氨气。
4、g,加水使溶解成100ml,再加稀氨溶液(1→30)调节pH值至0,即得。氨-氯化铵缓冲液(pH0)取氯化铵4g,加水20ml溶解后,加浓氯溶液35ml,再加水稀释至100ml,即得。这是我们常用的两种。
5、提高氯化铵浓度,降低氨水浓度。饱和氨水pH值能到17左右。氯化铵是强酸弱碱盐,弱酸性。
6、水溶液的pH:因为在水中电离出的铵根离子水解使溶液显酸性,常温下饱和氯化铵溶液PH值一般在6左右。25℃时,1%为5,3%为1,10%为0。
如何理解氯化铵水解反应?
1、很好理解。你只要知道平衡逆向移动就是抑制水解,正向就是促进。氯化铵水解生成一水合氨、氢离子。加入氢离子的话,溶液中氢离子的浓度就会增大,平衡就逆向移动,就会抑制水解。
2、弱电解质电离的等效平衡,一水合氨既然部分电离出铵根离子和氢氧根,那么,氯化铵电离出的铵根离子与氢氧根结合生成一水合氨。
3、很简单,氯化铵水解铵根离子和氯离子,铵根离子水解,结合了水电离出的氢氧根离子,所以溶液中的氢氧根离子就变少了,所以游离的氢离子的浓度>游离的氢氧根的浓度,溶液显酸性。
氯化铵水解时加盐酸,平衡怎么移动,水解程度有何变化
根据上面的离子方程式可知:HCl是强电解质,在水溶液中完全电离,向氯化铵溶液中加入盐酸使溶液中H^+浓度增大,氯化铵水解平衡逆反应方向移动,水解程度减弱。
氯化氨为强酸弱碱盐,溶液为酸性,你想,加了好多水,溶液就会趋向中性,c H 减小,kw不变,那么氢氧根离子浓度就增大。
抑制 因为氯化铵水解会产生氢离子,加入盐酸后氢离子浓度上升,水解平衡左移,所以是抑制水解 盐酸和氯化氢反应是因为氨水部分电离出氢氧根。
氯化铵在水中先电离成Cl-和NH4+,因为氯化铵是盐,是强电解质,完全电离,这是个不可逆的反应,不用考虑平衡。
氯化铵的水解反应
氯化铵水解方程式是:NH4Cl+H2ONH3·H2O+HCl。因为在水中电离出的铵根离子水解使溶液显酸性,常温下饱和氯化铵溶液pH值一般在6左右。25℃时,1%为5,3%为1,10%为0。
盐类的水解就是指盐中的弱碱阳离子或者酸根离子与水电离产生的氢离子或者氢氧根离子结合,生成弱电解质的过程。
反应后生成的是0.002mol的氯化铵和剩下的0.001mol的hcl。
硫化钠属于强碱弱酸盐,硫离子水解,溶液显碱性。Na2S+H2ONaHS+NaOH NaHS+H2OH2S+NaOH 氯化铵溶液中加入硫化钠,两者混合后可发生双水解反应,水解程度增大,有硫化氢和氨气溢出。
氯化铵水解离子方程式是NH4++H2O可逆生成NH3*H20+H+。氯化铵简称氯铵,是指盐酸的铵盐,多为制碱工业的副产品。
第一步:CO32-+H2O=== HCO3-+OH- 第二步:HCO3-+H2O=== H2CO3+OH- 氯化铵水解会产生盐酸和氨水(水解后呈酸性):NH4Cl+H2O=NH3·H2O+HCl 水解反应的性质:工业上应用较多的是有机物的水解,主要生产醇和酚。