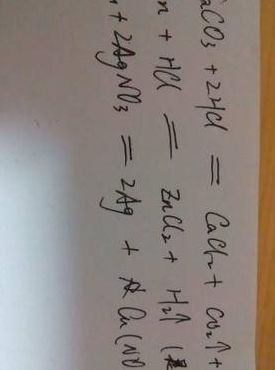求硝酸和硝酸银在光下分解的化学方程式
1、硝酸见光分解方程式:4hno3=(光)4no2+o2+2h2o 硝酸银见光分解方程式:4agno3 = (光)= 4ag + 4no2 + o2↑生成的银呈粉末状,黑色,沾上皮肤不易洗去。
2、硝酸见光分解的化学方程式为4HNO3=4NO2↑+O2+2H2O。稀硝酸见光一般不分解,浓度越稀,就越稳定。浓硝酸见光分解产生的二氧化氮溶解在浓硝酸中,会使溶液呈现黄色。硝酸是一种强酸,具有酸的通性。
3、硝酸银分解反应的化学方程式:2AgNO3=2Ag+2NO2↑+O2↑。
4、硝酸银见光分解,分解生成二氧化氮、氧气 、银。所有含银盐见光都会分解,所以一般都存放在棕色瓶中。
5、因此,试剂厂用银和硝酸反应制取硝酸银时,用稀硝酸而不用浓硝酸来溶解银。硝酸的性质与应用:浓硝酸不稳定,遇光或热会分解而放出二氧化氮,分解产生的二氧化氮溶于硝酸,从而使外观带有浅黄色 。但稀硝酸相对稳定。
硝酸银溶液多久见光分解
化学式AgNO3,无色透明斜方晶体。熔点212℃,相对密度352。在纯净空气中,硝酸银暴露在光线下并不分解和变色,但当存在有机物时,硝酸银见光就会变成灰色或灰黑色。
光对硝酸银滴定液影响不大 其主要原因不是光的影响,光的影响是非常小的,在我那种滴定环境和器材下。
③活泼金属硝酸盐(Ca前)分解得亚硝酸盐和O2 硝酸银加热至440℃时分解成银、氮气、氧气和二氧化氮。水溶液和乙醇溶液对石蕊呈中性反应,pH约为6。沸点 444℃(分解)。有氧化性。在有机物存在下,见光变灰色或灰黑色。
⒈能,这个,见光和加热都是提供给AgNO3分子能量的方法。。⒉提供能量。⒊不超过60℃?那你可能得需要另外外加手段,比如强光照射等等。。
硝酸银见光是可以分解的,因此不管是固体还是溶液都要保存的棕色的试剂瓶里面。
硝酸盐见光和受热都不稳定,像浓硝酸一样,容易分解,所以在高温下硝酸盐是强氧化剂。但它们的水溶液几乎没有氧化性。
为什么硝酸银的热分解温度高于硝酸铜的呢
铜之后的金属的氧化物也不稳定,加热时再分解为金属单质和氧气。硝酸盐热解原理 当加热到120℃时,它开始缓慢分解,温度高于180℃时则迅速分解:如果加热到300℃以上,或在起爆剂的影响下,即发生爆炸反应。
纯硝酸银对光稳定,但由于一般的产品纯度不够,其水溶液和固体常被保存在棕色试剂瓶中。硝酸银加热至444℃时分解成银、氮气、氧气和二氧化氮。水溶液和乙醇溶液对石蕊呈中性反应,pH约为6。沸点444℃(分解)。有氧化性。
③活泼金属硝酸盐(Ca前)分解得亚硝酸盐和O2 硝酸银加热至440℃时分解成银、氮气、氧气和二氧化氮。水溶液和乙醇溶液对石蕊呈中性反应,pH约为6。沸点 444℃(分解)。有氧化性。在有机物存在下,见光变灰色或灰黑色。
所以铜和硝酸银能够反应并且生成银河硝酸铜,硝酸银溶液原本呈无色,反应后析出铜离子,铜离子溶液为蓝色。所以反应后的溶液会呈现出蓝色。硝酸银遇有机物变灰黑色,分解出银。
硝酸银遇有机物变灰黑色,分解出银。纯硝酸银对光稳定,但由于一般的产品纯度不够,其水溶液和固体常被保存在棕色试剂瓶中。
硝酸银和硝酸都是无机化合物,它们的稳定性存在一定的差异。首先,硝酸属于强氧化酸,具有很强的氧化性,容易与有机物甚至一些无机物发生反应,而且在热、光等条件下也会分解,因此其稳定性相对较低。
硝酸银受热怎么分解及规律
1、硝酸银分解反应的化学方程式:2AgNO3=2Ag+2NO2↑+O2↑。
2、硝酸银加热会爆炸。加热至440℃即分解成金属银、氧、氮及氮的氧化物。接触有机物及硫化物时色泽变黑。可使蛋白质凝固,对人体有腐蚀作用。
3、那是因为他们的阳离子不同,惰性金属的阳离子得电子的能力比活泼金属的强,导致硝酸根受热分解的同时会受其氧化性的影响,所以活泼金属的硝酸盐分解一般是对应的亚硝酸盐如硝酸钠。
4、硝酸银加热至440℃时分解成银、氮气、氧气和二氧化氮。水溶液和乙醇溶液对石蕊呈中性反应,pH约为6。沸点 444℃(分解)。有氧化性。在有机物存在下,见光变灰色或灰黑色。硝酸银能与一系列试剂发生沉淀反应或配位反应。
5、电位定在铜以后的元素的硝酸盐受热分解则产生相应的金属单质,如:2agno3=2ag+2no2↑+o2↑。这里也可以认为在硝酸银开始热分解的温度,ag2o就已不稳定发生分解,故产物必为单质银。