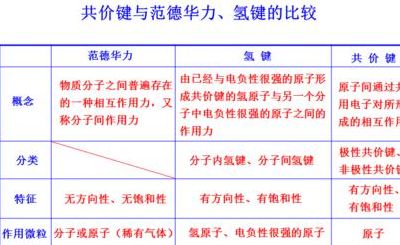
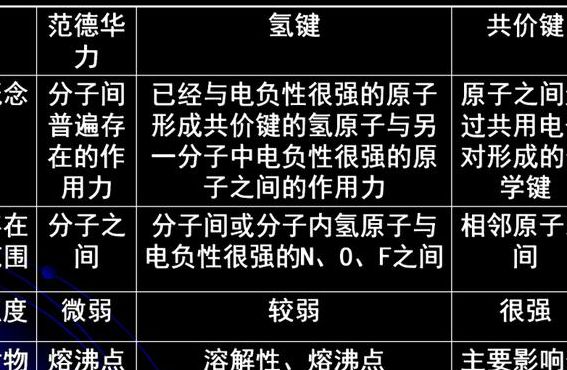
陶瓷内部原子间不存在哪种作用力?
1、范德华力又称分子间作用力。范德华力是存在于分子间的一种吸引力,它比化学键弱得多.一般来说,某物质的范德华力越大,则它的熔点、沸点就越高.对于组成和结构相似的物质,范德华力一般随着相对分子质量的增大而增强。
2、因为陶瓷内部不存在自由移动的电子,电子都被牢牢束缚在原子核周围,不能导电。金属内部则存在自由电子。
3、从晶体结构上看,金属原子因为半径一样大,采取密堆积方式,每个原子的成键数目多,因此每个金属键弱,再加上原子半径又大,形成形成的键弱。金属键离域程序高,使轨道能级差很小,导致电子在原子间流动非常容易。
4、不是。原子间作用力不是零,它是由电磁相互作用引起的,原子间作用力包括吸引力和斥力,决定了原子之间的相互作用和结合方式。
5、我们知道运动的电子会产生磁场,涡旋运动的电子形成的磁场会呈现为一个小磁针状态的可以分为正极和负极的磁场,也就是我们说的偶极子磁场。
6、氢原子中电子绕质子的轨迹一般为椭圆,质子在椭圆的焦点。
范德华能为什么有正负
形成原因不同 范德华键:分子中电子的运动产生瞬时偶极矩,它使临近分子瞬时极化,后者又反过来增强原来分子的瞬时偶极矩,这种相互耦合产生静电吸引作用。
由于高聚物中有很多长的分子链,因此积累起来导致范德华力很重要。另外范德华力又可以分为三种作用力:诱导力、色散力和取向力。
范德华力指的就是分子与分子之间的作用力。也就是俗称的分子间作用力,作用力的大小与相对分子质量呈正相关。分子的极性是指在一个分子当中,正电中心和负电中心不重合。要研究这个,就得知道分子的立体构型。
范德华力存在于分子之间。范德华力是分子之间普遍存在的一种相互作用力,它的本质是正负电荷间的相互吸引,它使得许多物质能以一定的凝聚态(固态或液态)存在。
范德华力是什么意思
1、范德华力是指分子间作用力,又称范德瓦尔斯力。是存在于中性分子或原子之间的一种弱碱性的电性吸引力。分子间作用力(范德瓦尔斯力)有三个来源:极性分子的永久偶极矩之间的相互作用。
2、解析:氯气、二氧化碳等常温是气体,在降低温度、增大压强时能凝结为液体,进一步能凝固为固体。状态之所以改变,是由于分子能缩短彼此间的距离,并由无规则运动转变为有规则排列,说明分子间存在作用力。该力为范德华力。
3、范德华力的定义 范德华力一般指分子间作用力即存在于中性分子或原子之间的一种弱碱性的电性吸引力,它比化学键弱得多。一般来说,某物质的范德华力越大,则它的熔点、沸点就越高。
4、指存在于分子(molecule)与分子之间或惰性气体(noble gas)原子(atom)间的作用力,又称范德华力(van der waals),具有加和性属于次级键。
5、范德华力是一种电性引力,它比化学健弱得多,通常每摩几个至数十个千焦。范德华力无饱和性和方向性,且永久存在于一切分子之间。范德华力也叫分子间力。
6、范德华力 (Van der Waals force) 范德瓦耳斯力(Van der Waals force),又称范氏引力或范德华力或凡得瓦力。在化学中,通常指分子之间的作用力。根据荷兰物理学家约翰尼斯·迪德里克·范·德·瓦尔斯命名。