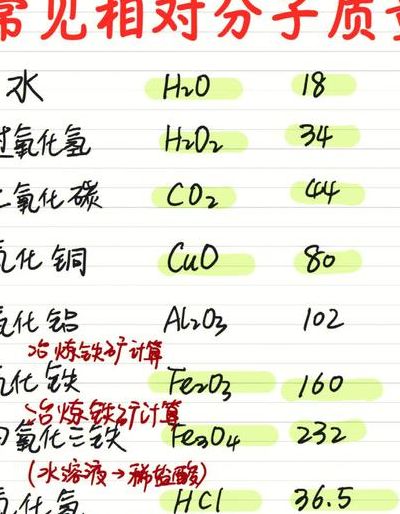
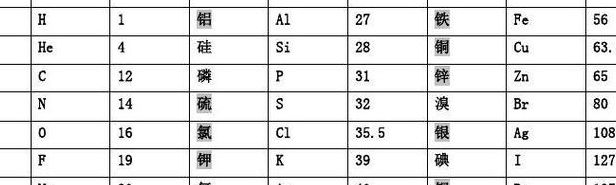
计算水,过氧化氢,氧化镁,瑞酸钾得相对分子质量
1、钠:23 钠是一种金属元素,在周期表中位于第3周期、第ⅠA族,是碱金属元素的代表,质地柔软,能与水反应生成氢氧化钠,放出氢气,化学性质较活泼。钠元素以盐的形式广泛的分布于陆地和海洋中,钠也是人体肌肉组织和神经组织中的重要成分之一。
2、H的相对原子质量为1,O的相对原子质量为16。因此,过氧化氢的相对分子质量为:相对分子质量 = 2×1 + 2×16 = 34 高锰酸钾(KMnO4)的相对分子质量:K的相对原子质量为31,Mn的相对原子质量为59,O的相对原子质量为16。
3、过氧化氢的相对分子质量是301。过氧化氢是一种无色黏稠的液体,具有很强的氧化性和漂白作用,因此被广泛用于漂白剂、氧化剂及生物实验等方面。在自然界的许多物质中,过氧化氢也广泛存在,例如空气中的氧气在紫外线的作用下会形成过氧化氢。过氧化氢的相对分子质量可以通过原子量加和的方式计算得到。
4、双氧水的分子式是H2O2,相对分子质量是34,一个H原子是1,一个O原子是16。双氧水是过氧化氢的水溶液,是无色无味的液体,具有较强的氧化性,但某些特殊条件下也可做还原剂,比如在和氯气、高锰酸钾等强氧化剂反应被氧化生成氧气时,其作还原剂。
5、相对分子质量就是相对原子质量之和。首先要理解化学式的含义,明确一个分子中含有几种原子,各有多少个,然后就好做了。
氧化镁的相对分子质量
氧化镁相对分子质量是40。氧化镁(Magnesiumoxide),是一种无机化合物,化学式为MgO,是镁的氧化物,是一种离子化合物,常温下为白色固体。氧化镁以方镁石形式存在于自然界中,是冶镁的原料。氧化镁有高度耐火绝缘性能。
氧化镁的相对分子质量是40,解释如下:氧化镁是一种常见的化学物质,其化学式为MgO。要计算其相对分子质量,我们需要将镁和氧的相对原子质量相加。我们知道镁的相对原子质量约为24,而氧的相对原子质量约为16。
MgO的相对分子质量为24+16=40。相对分子质量是一个分子中所有原子的相对原子质量的总和。在这个问题中,MgO代表氧化镁,它由镁(Mg)和氧(O)两种元素组成。首先,我们需要知道镁和氧的相对原子质量。镁的相对原子质量约为24,而氧的相对原子质量约为16。
氧化镁--MgO:其中Mg的相对原子质量为24,0为16;有1个Mg原子,所以Mg元素的相对原子质量为1*24=24;有1个o原子,所以0元素的相对原子质量,1*16=16。可得Mg元素与0元素的质量比为3:2。
钠:23 钠是一种金属元素,在周期表中位于第3周期、第ⅠA族,是碱金属元素的代表,质地柔软,能与水反应生成氢氧化钠,放出氢气,化学性质较活泼。钠元素以盐的形式广泛的分布于陆地和海洋中,钠也是人体肌肉组织和神经组织中的重要成分之一。
怎么计算氧化物的分子质量
1、二氧化碳的质量算法:CO是有 C 和 O 两种元素组成的,所以它的相对分子质量是:12 + 16 * 2 = 44。
2、O2的相对分子质量是32。单个氧原子的原子量是19994,一般取16,氧有三种同位素O1O1O18,三种同位素的的比例为O169762%、O170.038%、O180.2%。相对分子质量最小的氧化物的化学式为H2O,对于聚合物而言,其相对分子质量可达几万甚至几十万。
3、相对分子质量介绍:(Relative molecular mass),是指化学式中各个原子的相对原子质量(Ar)的总和,用符号Mr表示,单位是1。对于聚合物而言,其相对分子量可达几万甚至几十万;相对分子质量最小的氧化物的化学式为HO。
4、计算方法:分子中所有原子的相对原子质量之和。相对分子质量(Relativemolecularmass),即是指化学式中各个原子的相对原子质量(Ar)的总和,用符号Mr表示,单位是1。相对分子质量在数值上等于摩尔质量,但单位不同。
MgO相对分子质量
氧化镁相对分子质量是40。氧化镁(Magnesiumoxide),是一种无机化合物,化学式为MgO,是镁的氧化物,是一种离子化合物,常温下为白色固体。氧化镁以方镁石形式存在于自然界中,是冶镁的原料。氧化镁有高度耐火绝缘性能。
MgO的相对分子质量为24+16=40。相对分子质量是一个分子中所有原子的相对原子质量的总和。在这个问题中,MgO代表氧化镁,它由镁(Mg)和氧(O)两种元素组成。首先,我们需要知道镁和氧的相对原子质量。镁的相对原子质量约为24,而氧的相对原子质量约为16。
氧化镁的相对分子质量是40,解释如下:氧化镁是一种常见的化学物质,其化学式为MgO。要计算其相对分子质量,我们需要将镁和氧的相对原子质量相加。我们知道镁的相对原子质量约为24,而氧的相对原子质量约为16。
解:化学方程式为2Mg+O2=2MgO;Mg元素的相对原子质量为24,O元素的相对原子质量为16;所以上式中Mg与O的质量比为Mg:O=(2*24):(2*16)=3:2。所以24g镁和24g氧气反应时镁元素用完而氧气有剩余。