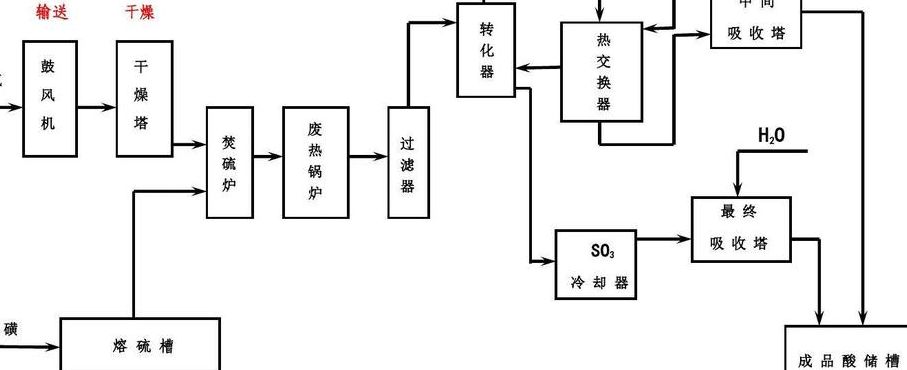
硫铁矿制硫酸(从矿石到化学品的转化过程)
硫铁矿制硫酸的原料主要包括硫铁矿、空气和水。硫铁矿通常需要经过破碎、磨细、浮选等工艺处理,以提高其含铁和含硫量。空气是氧化剂,用于将硫铁矿中的硫氧化为二氧化硫。水则用于稀释硫酸和冷却反应器。硫铁矿的热解反应 硫铁矿的热解反应是制备硫酸的第一步,它将硫铁矿中的硫和铁分离开来。
煅烧黄铁矿生产硫酸的过程如下:矿石准备:黄铁矿(也称为硫铁矿)是一种矿物,主要成分是二硫化亚铁(枯物FeS2)。首先,需要将黄铁矿进行粉碎和研磨,以便增加其表面积,提高反应效率。煅烧:将粉碎后的谈睁黄铁矿与氧气进行高温反应,生成二氧化硫(SO2)和三氧化硫(SO3)。
硫铁矿制硫酸的方程式为:4FeS2 + 11O2 2Fe2O3 + 8SO2;2SO2 + O2 2SO3;SO3 + H2O H2SO4。首先,硫铁矿(主要成分为FeS2)与氧气在高温下发生反应,生成三氧化二铁(Fe2O3)和二氧化硫(SO2)。
硫铁矿制硫酸方程式
硫铁矿分子式FeS2主要作用是制硫酸,其化学方程式是4FeS2+11O2=2Fe2O3+8SO2,2SO2+O2=2SO3,SO3+H2O=H2SO4。化学方程式比较简单但是实际工作较复杂,它在燃烧后生成的气体要进行除杂,通入高浓度氧气氧化而且最后要用吸收塔进行吸收。
硫铁矿制硫酸的方程式为:4FeS2 + 11O2 2Fe2O3 + 8SO2;2SO2 + O2 2SO3;SO3 + H2O H2SO4。首先,硫铁矿(主要成分为FeS2)与氧气在高温下发生反应,生成三氧化二铁(Fe2O3)和二氧化硫(SO2)。
FeS2+11O2=Fe3O4+6SO3 SO3+H2O=H2SO4 化学方程式比较简单但是实际工作较复杂,它在燃烧后生成的气体要进行除杂,通入高浓度氧气氧化而且最后要用吸收塔进行吸收。
SO2+O2==2SO3+47千卡(条件为在V2O5或在铂的催化下,同时在500摄氏度时SO2被氧化成SO3)接着在吸收塔内用百分之98浓硫酸来吸收SO3,生成H2S2O7(焦硫酸)接着用水稀释稀释成百分之98浓硫酸(H2S2O7+H2O=2H2SO4),然后成品。
硫铁矿 分子式 FeS2 主要作用是制硫酸 其化学方程式是 4FeS2+11O2=2Fe2O3+8SO2 2SO2+O2=2SO3 SO3+H2O=H2SO4生产6t百分之98的浓硫酸:1600*0.98=1568三式相加:4FeS2+15O2+8H2O=2Fe2O3+8H2SO4。
硫酸的制取方法
1、可将工业浓硫酸进行蒸馏,便可得到浓度95%~98%的商品硫酸。二水法磷酸反应后,利用磷石膏,工业循环利用,使用二水法制硫酸。方法二 制取二氧化硫(沸腾炉)2 4FeS2+11O2=高温=8SO2+2Fe2O3 将二氧化硫溶于水变成亚硫酸。亚硫酸氧化得硫酸。
2、可将工业浓硫酸进行蒸馏,便可得到浓度95%-98%的商品硫酸。二水法磷酸反应后,利用磷石膏,工业循环利用,使用二水法制硫酸。方法二:制取二氧化硫(沸腾炉)燃烧硫或高温处理黄铁矿,制取二氧化硫S+O2=点燃=SO2 4FeS2+11O2=高温=8SO2+2Fe2O3 将二氧化硫溶于水变成亚硫酸。
3、实验室制备硫酸的方法和化学方程式较多,这里简单列举两个比较容易制备的方法。