氢氧化锂可以用作什么
1、氢氧化锂可用做光谱分析的展开剂、润滑油。碱蓄电池电解质的添加剂,可增加电池容量12%~15%,提高使用寿命2~3倍。用做二氧化碳的吸收剂,可净化潜艇内的空气。
2、氢氧化锂可用做光谱分析的展开剂、润滑油。它作为碱性蓄电池电解质的添加剂,可增加电容量12%~15%,提高使用寿命2~3倍。它用做二氧化碳的吸收剂,可净化潜艇内的空气。
3、氢氧化锂是一种重要的无机化合物,主要用作制备其他化学品和分析试剂的原料。氢氧化锂的性质决定了它在多种领域的应用。以下是关于氢氧化锂的详细介绍:基本性质与应用领域概述 氢氧化锂是一种白色固体,具有强碱性和腐蚀性。
4、氢氧化锂在多个领域中发挥着重要作用。首先,它被用作光谱分析的辅助工具,作为展开剂,有助于提高分析的精确性。在电池技术上,氢氧化锂作为碱性蓄电池电解质的添加剂,能够显著提升电容器的容量,大约增加12%至15%,同时延长电池的使用寿命,大约提高2到3倍,这对于电池的性能优化至关重要。
5、氢氧化锂在多个领域有着广泛的应用。在光谱分析中,它可用作展开剂,帮助分离和检测不同的化合物。同时,它也被用作润滑油,具有一定的润滑性能。在电池领域,氢氧化锂作为碱性蓄电池电解质的添加剂,能够增加电容量12%~15%,提高电池的使用寿命2~3倍。
氢氧化锂是强碱还是弱碱?
氢氧化锂是强碱。氢氧化锂,是一种无机化合物,化学式为LiOH,为白色结晶性粉末,溶于水,微溶于乙醇,具有强碱性,氢氧化锂溶于水时完全电离成锂离子(Li+)和氢氧根离子(OH-),导致溶液中氢氧根离子浓度较高,所以氢氧化锂是强碱。氢氧化锂可用做光谱分析的展开剂、润滑油。
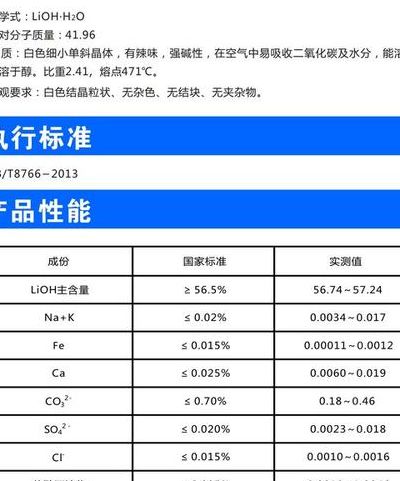
强碱性。氢氧化锂为白色单斜细小结晶。有辣味。具强碱性。在空气中能吸收二氧化碳和水分。溶于水,20摄氏度时溶解度为18g/100g水,微溶于乙醇,不溶于乙醚。
这个化学物质是强碱。氢氧化锂具有显著的碱性特征,能与多种酸反应生成相应的盐类,其水溶液呈现出强碱性,具有强烈的腐蚀性。在工业生产中,氢氧化锂广泛应用于电池制造、玻璃陶瓷、核工业等领域。需要注意的是,使用时要小心,避免与皮肤或眼睛接触,以免造成伤害。
氢氧化物可分为强碱,弱碱(包括中强碱)以及两性氢氧化物。
氢氧化锂属于强碱。氢氧化锂(Lithium hydroxide)是一种无机物,化学式为LiOH,为白色单斜细小结晶,有辣味,具强碱性,pKb = -0.04。在空气中能吸收二氧化碳和水分,可溶于水,20摄氏度时溶解度为18g/100gH2O,微溶于乙醇,不溶于乙醚。1mol/L溶液的pH约为14。
氢氧化锂被归类为强碱。它展现出明显的碱性,并能与多种酸发生反应,生成相应的盐类。其水溶液呈现出强烈的碱性,并具有显著的腐蚀性。在工业上,氢氧化锂被广泛应用于电池制造、玻璃和陶瓷生产、以及核工业等领域。使用时需谨慎,防止与皮肤或眼睛接触,以免造成伤害。
氢氧化锂为什么不是四大强碱
1、有弱酸性。强碱是指在水溶液中电离出的阴离子全部是氢氧根离子的物质,氢氧化锂则是含有弱酸性,因此不是四大强碱。
2、大强碱:氢氧化锂[LiOH]、氢氧化钠[烧碱,NaOH]、氢氧化钾[KOH]、氢氧化铷[RbOH]。硝酸是一种具有强氧化性、腐蚀性的强酸,属于一元无机强酸,是六大无机强酸之一,也是一种重要的化工原料。在工业上可用于制化肥、农药、炸药、染料、盐类等。
3、四大强碱:氢氧化钾K(OH)、氢氧化钠Na(OH)、氢氧化钡Ba(OH)、氢氧化钙Ca(OH)因为非金属性越强酸性越强,金属性越强,碱性越强。
4、高中化学中,强碱有四个,称为四大强碱:氢氧化钾、氢氧化钠、氢氧化钙、氢氧化钡可溶性弱碱只有一个就是氨水其他均为不溶性弱碱(氢氧化镁为中强碱。做题时可视为弱碱对待)其实在化学中,还有很多强碱,例如碱金属元素形成的氢氧化物都是强碱。氢氧化锂、氢氧化铯等。
氢氧化锂是强碱还是弱碱
氢氧化锂是强碱。氢氧化锂,是一种无机化合物,化学式为LiOH,为白色结晶性粉末,溶于水,微溶于乙醇,具有强碱性,氢氧化锂溶于水时完全电离成锂离子(Li+)和氢氧根离子(OH-),导致溶液中氢氧根离子浓度较高,所以氢氧化锂是强碱。氢氧化锂可用做光谱分析的展开剂、润滑油。
强碱性。氢氧化锂为白色单斜细小结晶。有辣味。具强碱性。在空气中能吸收二氧化碳和水分。溶于水,20摄氏度时溶解度为18g/100g水,微溶于乙醇,不溶于乙醚。
氢氧化锂属于强碱。氢氧化锂(Lithium hydroxide)是一种无机物,化学式为LiOH,为白色单斜细小结晶,有辣味,具强碱性,pKb = -0.04。在空气中能吸收二氧化碳和水分,可溶于水,20摄氏度时溶解度为18g/100gH2O,微溶于乙醇,不溶于乙醚。1mol/L溶液的pH约为14。
强碱和弱碱有哪些?
强酸:H2SOHCl、HNOHI、HClOHClO4。强碱:NaOH、KOH、Ba(OH)Ca(OH)2。弱酸:H3POH2SOHF、H2COH2S、CH3COOH、HClO、HIOH2C2O4(草酸)、HNOHCN。弱碱:NH3·H2O、Fe(OH)Fe(OH)Si(OH)Al(OH)3。
强碱包括氢氧化钠、氢氧化钾、氢氧化钙)等。弱碱则有氨水、氢氧化铝)、氢氧化镁)等。强碱和弱碱的定义及特性 强碱指的是在水溶液中能完全解离的碱。如氢氧化钠,它解离出的氢氧根离子浓度较高,具有显著的碱性。这类碱在化学反应中表现出强烈的性质,如腐蚀性和刺激性。
强碱是指在水溶液中完全解离成金属离子和氢氧根离子的物质。常见的强碱有氢氧化钠、氢氧化钾、氢氧化钙)、氢氧化钡)等。这些强碱在溶液中表现出强烈的碱性,能够完全解离,产生大量的氢氧根离子。弱碱 弱碱是指在水溶液中只能部分解离成金属离子和氢氧根离子的物质。
氢氧化物可分为强碱,弱碱(包括中强碱)以及两性氢氧化物。
强碱包括: 氢氧化钠(NaOH)、氢氧化钾(KOH)、氢氧化钙(Ca(OH))、氢氧化钡(Ba(OH))。弱碱包括: 氨水(NHHO)、氢氧化铝(Al(OH))、氢氧化铜(Cu(OH))、氢氧化锌(Zn(OH))。
化学常见的强碱:可溶性的有三种:氢氧化钾 氢氧化钠 氢氧化钡 微溶的有一种 氢氧化钙 弱碱 :氢氧化铁。