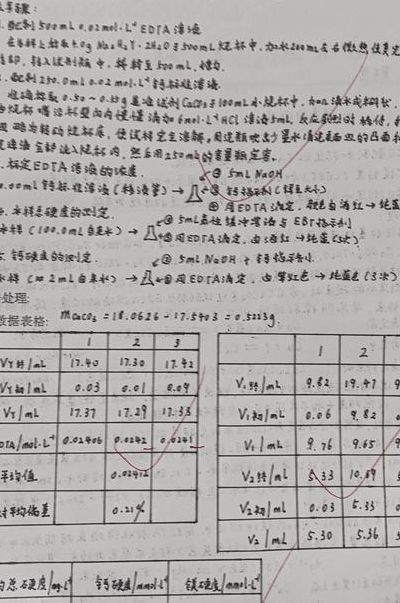
谁能给我水的总硬度测定的实验报告和演示
了解配位滴定法基本原理和方法。了解水的硬度的概念及其表示方法。实验原理 含有钙、镁离子的水叫硬水。
水的总硬度测定是化学分析中的一个重要实验,旨在了解水硬度的概念及其表示方法,同时掌握配位滴定的基本原理和方法。本实验通过测定水中钙、镁离子的总含量,来确定水的硬度。实验基于EDTA配位滴定法,该方法在滴定时,溶液颜色会从红色转变为蓝色,这标志着滴定终点的到达。
硬度测量实验报告旨在探索材料性能的关键指标之一——硬度。硬度测试不仅能够评估材料抵抗硬物压入其表面的能力,而且由于其简便性和无损性,在生产和科研领域有着广泛的应用。实验报告将详细介绍硬度测量的原理及常用方法。
泉景净水机10大演示方法 测试TDS值 自来水的TDS值一般在100-500之间,通过RO机过滤之后,TDS值会变为5-30之间。说明:RO膜能过滤水中的大部分杂质,效果显著。注意:超滤不能测TDS值,数值没有变化,影响消费者购买。
米扬净水机通过多种演示方法展示了其出色的性能。首先,测试TDS值,RO机过滤后TDS值显著降低,显示其能有效去除杂质。电解法对比显示,RO膜能有效过滤杂质,而超滤机则无法通过此方法体现效果。硬度测试中,RO膜能有效降低水的硬度,但超滤机对此无明显改善。
水中钙离子和镁离子含量及水硬的测定实验中产生误差的原因
分析方法和仪器的误差:分析方法和仪器的精度直接影响着实验结果的准确性。如果使用的分析方法不准确或者使用的仪器精度不高,就会对测定结果产生误差。水样取样和处理的误差:所测水样的取样和处理也造成误差。比如说,如果取样的时间不对,会导致水样中离子含量的变化。
如用基准氯化锌标定,则分析方法不一致,即分析的元素、缓冲溶液、PH值、指示剂、空白等等的不一致,导致较大的系统误差。镁离子与指示剂铬黑T的反应较钙离子灵敏,故常在滴定时加入少量的Mg2+-EDTA,使终点突跃。钙、镁是水中最常见离子,蒸馏水(去离子水)要严格处理。
测定水中钙镁含量时,控制溶液的pH值在10左右可以提高滴定的灵敏度。如果pH值过高,容易导致钙镁离子沉淀;而pH值过低时,镁离子与指示剂的络合较松散,可能导致滴定终点提前,从而引起较大偏差。因此,根据实际测定EDTA的酸效应,pH=10被认为是测定钙镁离子的最佳条件。
工业用水的总硬度测定的实验报告和演示
1、了解配位滴定法基本原理和方法。了解水的硬度的概念及其表示方法。实验原理 含有钙、镁离子的水叫硬水。
2、水的总硬度测定是化学分析中的一个重要实验,旨在了解水硬度的概念及其表示方法,同时掌握配位滴定的基本原理和方法。本实验通过测定水中钙、镁离子的总含量,来确定水的硬度。实验基于EDTA配位滴定法,该方法在滴定时,溶液颜色会从红色转变为蓝色,这标志着滴定终点的到达。
3、洛氏硬度计,主要用于金属材 料热处理后的产品性能检验。布氏硬度计,应用于黑色、有色金属材料检验,也可测一般退 火、正火后试件的硬度。
用EDTA法怎么测定水的总硬度?用什么作指示剂?溶液的PH值应控制在什么...
水的总硬度=[Ca2+] + [Mg2+]. 可以用铬黑T作为指示剂,在pH=10的氨缓冲溶液中用EDTA直接滴定。另取一份样品。不用缓冲溶液,pH=13 时,Mg(OH)2沉淀,这时,EDTA只能滴定 Ca2+。
在采用EDTA进行水的硬度测定时,溶液的pH值需严格保持在12±0.1的范围内。EDTA络合滴定法是一种广泛应用的化学分析方法,用于测定水的总硬度。该方法基于在特定条件下,使用铬黑T作为指示剂和氨-氯化铵作为缓冲溶液,通过EDTA与水中的钙、镁离子反应形成稳定的络合物,以此确定水中钙镁离子的总量。
在使用EDTA滴定法测定水的总硬度时,控制溶液的酸度是至关重要的。通常,我们采用氨-氯化铵缓冲溶液或硼砂缓冲溶液来确保溶液的pH值维持在10±0.1的范围内,这对于滴定过程的准确性至关重要。
用edta法怎样测定水的总硬度如下:配制EDTA溶液:称取乙二胺四乙酸二钠盐,溶于水中,可适当加热溶解,冷却后转移至试剂瓶中,用水稀释至刻度,摇匀。绘制标准曲线:分别吸取一定浓度的钙离子和镁离子标准溶液,用EDTA溶液滴定,记录滴定量,绘制标准曲线。
用EDTA测定水的总硬度时,以氨-氯化铵缓冲溶液,或硼砂缓冲溶液来控制溶液酸碱度(pH=10±0.1)。如果水样酸性或碱性太高时,可用氢氧化钠溶液或稀盐酸中和后,再用缓冲溶液来调整选择铬黑T或酸性铬蓝K作指示剂。
用EDTA法测定钙镁离子的含量,其原理与以CaCO为基准物质标定edta标准溶液浓度相同,总硬则以铬黑t为指示剂,加入5mlNH-NHCl 缓冲溶液,控制溶液的ph值为10。以EDTA标准溶液滴定。发生络合反应。溶液颜色由酒红色滴定至纯蓝色,即为终点。