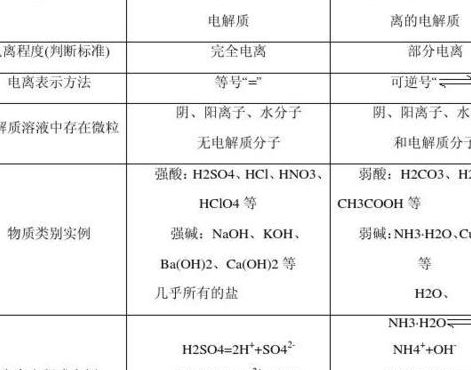
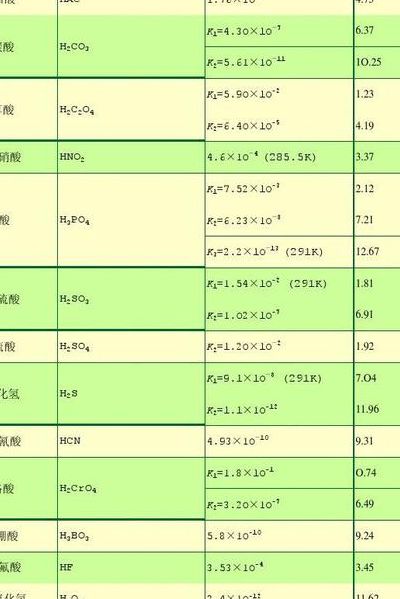
都有哪些盐类物质属于弱电解质
常见的弱电解质包括弱酸如H2S、H2COCH3COOH、HF、HCN、HClO等。HF酸由于其强极性共价键,被归类为弱电解质。即便H3POH2SO3表现出较强的酸性,它们依然属于弱电解质范畴。
常见的弱电解质盐主要包括醋酸盐。醋酸盐在水溶液中电离出的醋酸根离子与其相对应的阳离子无法完全解离,表现出一定程度的弱导电性。磷酸盐也属于常见的弱电解质盐之一。另外,部分硅酸盐也具有弱电解质的特性。这些物质由于其特殊的分子结构,导致在水溶液中只能部分电离,因此表现出弱电解质的性质。
弱电解质方面,氢氟酸(HF)、氢硫酸(H2S)、醋酸(CH3COOH)都属于弱酸。弱碱则包括氢氧化铁(Fe(OH)3)、氢氧化亚铁(Fe(OH)2)、氨水(NH3·H2O)以及一些难溶性的碱类物质。
高中常见的弱电解质有哪些
高中化学常见的强电解质主要有:(1)强酸,如,H2SOHCl、HNOHBr、HI等;(2)强碱,如,NaOH、KOH、Ba(OH)2等;(3)大部分盐,中学常见的盐基本都是。
高中化学中,常见的弱电解质包括多种酸和碱。其中,常见的弱酸有碳酸、醋酸、苯甲酸等。弱酸在水中的电离程度较低,电离产生的离子较少。强电解质则包括所有可溶的盐,例如硫酸(H2SO4)、硝酸(HNO3)、高氯酸(HClO4)等。这些酸完全电离,产生的离子较多。
高中常见的弱电解质有H2S、H2COCH3COOH、HF(氢氟酸)、HCN、HClO(次氯酸)、氢氧化铝,氢氧化锌、HgClPb(Ac)HgBrCdI水。弱电解质是在水溶液中不完全(少部分)电离的电解质。弱电解质在水溶液中既有分子存在又有离子存在。水是一种特殊的弱电解质。
常见的弱电解质有哪些?
1、高中化学常见的强电解质主要有:(1)强酸,如,H2SOHCl、HNOHBr、HI等;(2)强碱,如,NaOH、KOH、Ba(OH)2等;(3)大部分盐,中学常见的盐基本都是。
2、弱电解质有CH3COOH、HF、H2COH2SOH2S、HClO、HCN、氢氧化铝、氢氧化、HgCl水等。弱电解质一般有弱酸、弱碱,少部分盐。弱电解质是在水溶液里部分电离的电解质,包括弱酸。弱碱一水合氨(氨水)两性氢氧化物:氢氧化铝,氢氧化锌。个别的盐如HgClPb(Ac)HgBrCdI2等。
3、弱酸 H2S、H2COCH3COOH、HF、HCN、HClO(次氯酸)等。弱碱 一水合氨(氨水) 两性氢氧化物:氢氧化铝,氢氧化锌。个别的盐 如HgClPb(Ac)HgBrCdI2等 水 是由强极性键构成的极弱的电解质。常见的弱电解质举例:醋酸:0.1 mol·L-1的CH3COOH溶液的pH1。
4、常见的强电解质和弱电解质有:sococh3ch2oh、c12h22o11(蔗糖)。弱电解质有CH3COOH、HF、H2COH2SOH2S、HClO、HCN、氢氧化铝、氢氧化、HgCl水等。弱电解质一般有弱酸、弱碱,少部分盐。弱电解质是在水溶液里部分电离的电解质,包括弱酸。
5、弱电解质主要包括弱酸,如碳酸(H2CO3)、亚硫酸(H2SO3)、醋酸(CH3COOH)、氢硫酸(H2S)、氢氟酸(HF)、硅酸(H2SiO3)、原硅酸(H3SiO4)、所有有机酸等。弱碱包括一水合氨(NHH2O)和除强碱外的所有氢氧化金属R(OH)3等。水(H2O)也是一种弱电解质。
6、弱电解质是一类具有极性键的共价化合物。这些化合物通常包括弱酸如HClO、HCN、H2S等,弱碱如NH3·H2O、Cu(OH)Fe(OH)2,以及两性氢氧化物如Al(OH)Zn(OH)2,还有少数盐如Pb(CH3COO)2。与之相对,一些具有极性键的共价化合物则不是电解质,例如SOCOCH3CH2OH、C12H22O11(蔗糖)等。
常见的弱电解质有哪些
1、弱电解质有CH3COOH、HF、H2COH2SOH2S、HClO、HCN、氢氧化铝、氢氧化、HgCl水等。弱电解质一般有弱酸、弱碱,少部分盐。弱电解质是在水溶液里部分电离的电解质,包括弱酸。弱碱一水合氨(氨水)两性氢氧化物:氢氧化铝,氢氧化锌。个别的盐如HgClPb(Ac)HgBrCdI2等。
2、弱电解质指的是那些含有极性键的共价化合物,它们在溶液中的电离程度较小。例如,HClO、HCN和H2S等弱酸,NH3·H2O、Cu(OH)2和Fe(OH)2等弱碱,以及Al(OH)Zn(OH)2等两性氢氧化物,还有少数盐如Pb(CH3COO)2,都属于弱电解质。
3、高中化学常见的强电解质主要有:(1)强酸,如,H2SOHCl、HNOHBr、HI等;(2)强碱,如,NaOH、KOH、Ba(OH)2等;(3)大部分盐,中学常见的盐基本都是。
4、弱电解质包括弱酸和弱碱。其中,弱酸有碳酸(H2CO3)、亚硫酸(H2SO3)、醋酸(CH3COOH)、氢硫酸(H2S)、氢氟酸(HF)以及硅酸(H2SiO3)和原硅酸(H3SiO4)。当然,所有的有机酸也都属于弱酸类别。在弱碱中,一水合氨(NHH2O)和除强碱之外的所有金属氢氧化物(R(OH))均属于弱碱的范畴。
5、常见的强电解质和弱电解质有哪些如下:常见的强电解质和弱电解质有:sococh3ch2oh、c12h22o11(蔗糖)。弱电解质有CH3COOH、HF、H2COH2SOH2S、HClO、HCN、氢氧化铝、氢氧化、HgCl水等。弱电解质一般有弱酸、弱碱,少部分盐。弱电解质是在水溶液里部分电离的电解质,包括弱酸。
6、HClO(次氯酸)等。弱电解质有CH3COOH、HF、H2COH2SOH2S、HClO、HCN、氢氧化铝、氢氧化、HgCl水等。弱电解质一般有弱酸、弱碱,少部分盐。弱电解质是在水溶液里部分电离的电解质,包括弱酸。弱碱一水合氨(氨水)两性氢氧化物:氢氧化铝,氢氧化锌。个别的盐如HgClPb(Ac)HgBrCdI2等。
弱电解质有哪些物质?
1、弱电解质包括水、弱酸、弱碱和部分有机化合物。以下是详细的解释:弱电解质是指在水中或其他溶剂中,只有部分分子能够解离成离子的化合物。这些化合物在水溶液中不完全电离,表现出相对较低的导电性。水是最常见的弱电解质。尽管水的电离程度很低,但它仍然会部分地解离成氢离子和氢氧根离子。
2、弱电解质包括:弱酸 H2S、H2COCH3COOH、HF、HCN、HClO(次氯酸)等。弱碱 一水合氨(氨水) 两性氢氧化物:氢氧化铝,氢氧化锌。个别的盐 如HgClPb(Ac)HgBrCdI2等 水 是由强极性键构成的极弱的电解质。
3、弱电解质是指那些在水溶液中只能部分电离的极性共价化合物。这类化合物不同于完全不导电的非电解质,如SOCO2和一些有机物,如CH3CH2OH和C12H22O11(蔗糖)。
4、高中化学常见的强电解质主要有:(1)强酸,如,H2SOHCl、HNOHBr、HI等;(2)强碱,如,NaOH、KOH、Ba(OH)2等;(3)大部分盐,中学常见的盐基本都是。
5、弱电解质的物质包括:醋酸、氨水、氢氟酸等弱酸或弱碱。弱电解质指的是在水溶液中或熔融状态下不完全电离的化合物。与强电解质不同,弱电解质在水中的电离程度较小,因此存在未电离的分子状态。以下是对弱电解质具体例子的详细解释: 弱酸:常见的弱酸如醋酸(CH3COOH)。
6、弱电解质包括:醋酸、氨水、氢氟酸等。弱电解质是指在水中不能完全电离的电解质。它们与强电解质相比,电离程度较小,分子部分电离成离子。弱电解质主要包括以下几种: 醋酸:醋酸是常见的弱电解质之一。它在水中的电离程度较低,只能部分电离成醋酸根离子和氢离子。